26. Теплоемкость. Применение первого начала к изопроцессам:
изобарный. изохорный,
изотермический.
Удельная
теплоемкость вещества — величина, равная количеству теплоты, необходимому
для нагревания 1 кг вещества на 1 К:
![]()
Молярная
теплоемкость—величина, равная количеству теплоты, необходимому для
нагревания 1 моль вещества на 1 К:
![]() (1)
(1)
где ν=m/М—количество вещества.
Единица молярной теплоемкости — джоуль на моль•кельвин (Дж/(моль•К)).
Первое начало термодинамики, выражая закон сохранения и превращения энергии, не позволяет установить направление протекания термодинамических процессов.
Изохорный процесс (V = const). При изохорном процессе газ не совершает работы над внешними телами, т. е.
dA=pdV = 0. из первого начала термодинамики (dQ=dU+dA) для изохорного процесса следует, что вся теплота, сообщаемая газу, идет на увеличение его внутренней энергии:
dQ =dU
Согласно формуле , dUm = CvdT.
Изобарный процесс (р=const). При изобарном процессе работа газа при расширении объема от V1 до V2 равна
![]()
Если использовать уравнение Клапейрона — Менделеева
![]()
откуда
![]()
Тогда выражение для работы изобарного расширения примет вид
![]()
Из этого выражения вытекает физический смысл молярной газовой постоянной R: если T2 —T1 =1 К, то для 1 моль газа R=A, т. е. R численно равна работе изобарного расширения 1 моль идеального газа при нагревании его на 1 К.
В изобарном процессе при сообщении газу массой т количества теплоты
![]()
его внутренняя энергия
возрастает на величину ![]()
Изотермический процесс (T=const), изотермический процесс описывается законом Бойля—Мариотта:
работу изотермического расширения газа:
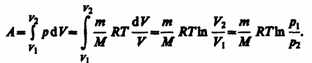
Так как при Т=const внутренняя энергия идеального газа не изменяется:
![]()
то из первого начала термодинамики (dQ=dU+dA) следует, что для изотермического процесса
![]()
т. е. все количество теплоты, сообщаемое газу, расходуется на совершение им работы против внешних сил:
![]()
Следовательно, для того чтобы при расширении газа температура не понижалась, к газу в течение изотермического процесса необходимо подводить количество теплоты, эквивалентное внешней работе расширения.